درس دوم علوم نهم
فصل دوم :
رفتار اتم ها با یکدیگر
یاد آوری
مواد در طبیعت به سه حالت جامد، مایع و گاز هستند. اتم ها، ذرات تشکیل دهنده مواد هستند و هر اتم از سه ذره الکترون پروتون و نوترون تشکیل شده است. پروتون و نوترون در هسته اتم قرار دارند و الکترون ها در مدار های مشخصی در اطراف هسته اتم در حال گردش اند و می توانند در شرایط خاصی از یک اتم جدا شده و به اتم دیگر منتقل شوند. در حالت عادی تعداد الکترون و پروتون هر اتم برابر است ولی چنانچه تحت شرایطی اتمی الکترون از دست بدهد یا بگیرد تبدیل به یون می شود .

انواع مواد خالص:
1)عنصر: مواد خالصی هستند که فقط از یک نوع اتم تشکیل شده اند. مانند مس، طلا، اکسیژن و...
2)ترکیب: مواد خالصی هستند که مولکول آنها از دو یا چند اتم متفاوت تشکیل شده است، مانند نمک، شکر، آب و...


کاربرد چند ترکیب در زندگی:
اتیلن گلیکول : به عنوان ضد یخ در رادیاتور اتوموبیل
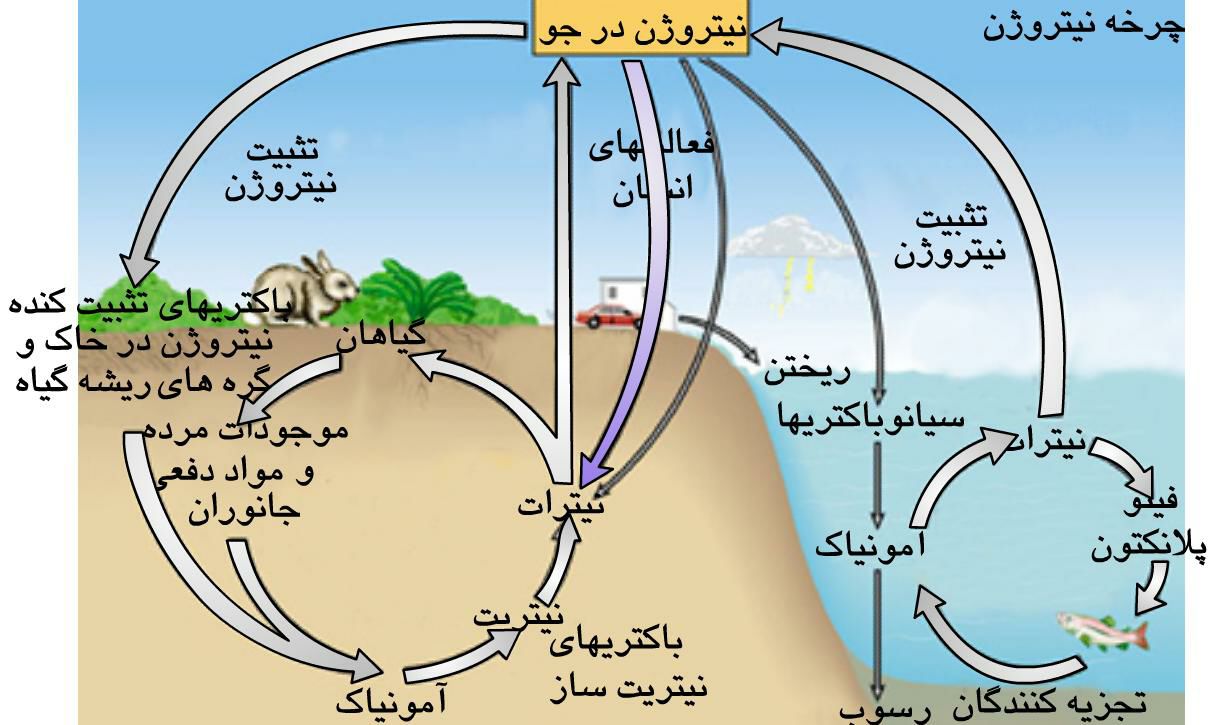
آمونیاک : به عنوان کود برای رشد گیاهان
اتانول : به عنوان ضد عفونی کننده وسایل پزشکی
آب آهک : ضد عفونی کنند – تُرد کردن کدو حلوایی برای تهیه مربا

نکته: مواد معمولا در طبیعت به شکل خالص یافت نمی شوند مانند این تکه سنگ که در آن رگه هایی از طلا وجود دارد .

نحوه تشکیل ترکیبات یونی
انواع یون: یون مثبت (کاتیون) یون منفی (آنیون)
پیوند یونی: پیوندی است که بین یون های مثبت و منفی ایجاد می شود. همانطور که در تصویر زیر می بینید از واکنش فلز سدیم و گاز کلر،سدیم کلرید بوجود می آید، اگر تعداد الکترون های سدیم و کلر را قبل و بعد از واکنش با همدیگر مقایسه کنیم متوجه می شویم که سدیم یک الکترون از دست داده و تبدیل به یون مثبت (کاتیون) شده و کلر یک الکترون گرفته و تبدیل به یون منفی (آنیون) شده است .
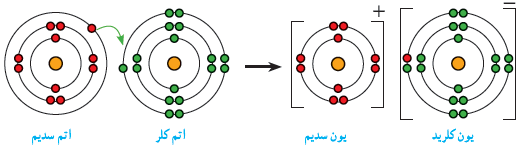
با توجه به واکنش سدیم و کلر:
1)اتم سدیم با از دست دادن یک الکترون مدار آخر خود، به یون مثبت تبدیل شده است .
2)اتم کلر با گرفتن یک الکترون از سدیم، به یون منفی تبدیل شده است و تعداد الکترون های مدار آخر خود را به 8 رسانده است.
3)فلز ها تمایل به از دست دادن الکترون دارند .
4) نافلز ها تمایل به گرفتن الکترون دارند .
نکته: یون ها می توانند در یک محلول حرکت کنند و به طور مساوی در همه جای محلول پخش شوند و جریان الکتریکی را در آن محلول برقرار سازند .
نکته : یون ها در حالت جامد رسانا نیستند و سخت و شکننده می باشند .
مشارکت الکترونی و پیوند کووالانسی
همانطور که در تصویر می بینید که از ترکیب یک اتم اکسیژن با دو اتم هیدروژن یک مولکول آب به وجود می آید. با توجه به شکل پایین در این ترکیب انتقال الکترون صورت نمی گیرد بلکه تعدادی از الکترون های مدار آخر خود را به اشکتراک می گذارند. وقتی که دو اتم نافلز مناسب در کنار هم قرار می گیرند یک یا چند الکترون مدار آخر خود را با یکدیگر به اشتراک می گذارند و پیوندی بین آنها برقرار می شود که به آن پیوند کووالانسی می گویند .

نکته: با دقت در ترکیب مولکولی آب کتوجه می شویم که برخی از اتم ها فقط می توانند یک پیوند کووالانسی برقرار کند مانند هیدروژن ولی برخی از اتم ها دو یا چند پیوند کووالانسی برقرار می کنند مانند اکسیژن. نیتروژن سه پیوند کووالانسی و کربن چهار پیوند کووالانسی بر قرار کند .
انواع پیوند:
پیوند یونی: پیوندی است که به واسطه انتقال الکترون بین دو ذره صورت می گیرد
یعنی پیوند بین یون مثبت و یون منفی مانند پیوندی که بین فلز ها و نافلزها می تواند ایجاد شود
پیوند کووالانسی: پیوندی است که از به اشتراک گذاشتن تعدادی از الکترون های مدار آخر بین دو اتم ایجاد می شود؛ مانند پیوند بین دو نافلز اکسیژن و هیدروژن
نکته: به موادی که از پیوند یونی حاصل می شوند، ترکیب یونی به موادی که از پیوند کووالانسی به وجود می آیند، ترکیب مولکولی می گویند .
چند نکته مهم :
1)اگر ترکیب های یونی را در آب حل کنیم یون های مثبت و منفی آنها از هم جدا می شوند و این ذره ها در کل محلول پخش می شوند به همین دلیل می توانند جریان الکتریکی را از خود عبور دهند .
2)موادی که ترکیب مولکولی دارند جریان برق ره به راحتی عبور نمی دهد زیرا به صورت مولکولی در آب حل می شوند و یون ایجاد نمی کنند.
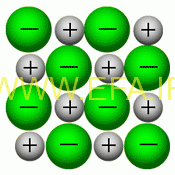
3)یون ها در ترکیب های یونی به صورت شبکه ای به هم متصل هستند و هر یون توسط چند یون غیر هم نام خود احاطه می د و بین آنها نیروی جاذبه قوی ایجاد می شود. به همین دلیل ترکیبات یونی در حالت جامد، رسانای جریان برق نیستند ولی در حالت مذاب یا محلول، مقتی که یون ها از هم جدا می وند می توانند جریان برق را عبور دهند .
بسیار مهم: ترکیب های یونی در مجموع از نظر بار الکتریکی خنصی هستند .
پایان فصل دوم